三硫化二砷
外觀
| 三硫化二砷 | |
|---|---|

| |
| |
| IUPAC名 Arsenic trisulfide | |
| 別名 | 硫化砷(III)、雌黃 |
| 識別 | |
| CAS編號 | 1303-33-9 |
| PubChem | 4093503 |
| ChemSpider | 21241348 |
| SMILES |
|
| InChI |
|
| InChIKey | OUFDYFBZNDIAPD-UHFFFAOYAM |
| EINECS | 215-117-4 |
| RTECS | CG2638000 |
| 性質 | |
| 化學式 | As2S3 |
| 摩爾質量 | 246.04 g·mol−1 |
| 外觀 | 橙色晶體 |
| 密度 | 3.43 g cm−3 |
| 熔點 | 310 °C(583 K) |
| 沸點 | 707 °C(980 K) |
| 結構 | |
| 空間群 | P21/n (No. 11) |
| 晶格常數 | a = 1147.5(5) pm, b = 957.7(4) pm, c = 425.6(2) pm |
| 晶格常數 | α = 90°, β = 90.68(8)°, γ = 90° |
| 配位幾何 | As:角錐型 |
| 危險性 | |
| H-術語 | H300, H331, H400, H411 |
| NFPA 704 | |
| PEL | [1910.1018] TWA 0.010 mg/m3 |
| 相關物質 | |
| 其他陰離子 | 三氧化二砷 三硒化二砷 |
| 其他陽離子 | 三硫化二磷 硫化銻 硫化鉍 |
| 相關化學品 | 四硫化四砷 |
| 若非註明,所有數據均出自標準狀態(25 ℃,100 kPa)下。 | |
三硫化二砷是一種無機化合物,化學式為As2S3。三硫化二砷在自然界以雌黃礦物的形式存在。[1]
結構
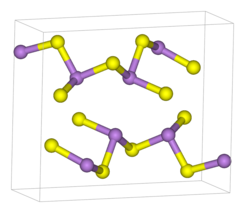
[編輯]三硫化二砷存在晶體和無定形體。[2]單斜的As2S3是層狀結構,每個As和3個S成鍵,As-S為224pm,∠S-As-S 99°;而其蒸氣以二聚體As4S6的形式存在,結構與As4O6類似。[3]
屬性
[編輯]它是一種半導體,直接的能隙為2.7 eV[4]。 寬的能隙使它對於620 nm至11 µm的紅外線透明。
製備
[編輯]三硫化二砷可由單質化合得到,或者從As(III)的溶液中由H2S沉澱。[5]
- 2 As + 3 S → As2S3
化學性質
[編輯]- 2 As2S3 + 9 O2 → 2 As2O3 + 6 SO2
它可以被硫化鈉轉化為三硫代亞砷酸鈉,被多硫化鈉轉化為四硫代砷酸鈉:
- As2S3 + 3 Na2S → 2 Na3AsS3
- As2S3 + 3 Na2S2 → 2 Na3AsS4
而在和氫氧化鈉溶液的反應中,會同時產生亞砷酸鹽和硫代亞砷酸鹽:
- As2S3 + 6 NaOH → Na3AsO3 + Na3AsS3 + 3 H2O
此溶液在經過脫硫、還原等操作可以製得三氧化二砷。[6]當溶液中OH-不足時,則產生偏亞砷酸鹽和硫代偏亞砷酸鹽:[7]
- 2 As2S3 + 4 NaOH → NaAsO2 + 3 NaAsS2 + 2 H2O
和碳酸鈉溶液反應,得到同樣的砷化合物:
- 2 As2S3 + Na2CO3 → NaAsO2 + 3 NaAsS2 + 2 CO2↑
- As2S3 + 6 Cl2 → (AsCl3)2·3SCl2
- As2S3 + 3 I2 → 2 AsI3 + 3 S
和氯化亞銅、氯化銀等金屬氯化物共熱,均會產生三氯化砷:[7]
- 3 As2S3 + 6 CuCl —200~300℃→ Cu6As4S9 + 2 AsCl3 (CuCl過量則產生Cu4As2S5)
- 2 As2S3 + 3 AgCl —170℃→ 3 AgAsS2 + AsCl3
- 2 As + 3 Hg2Cl2 → 2 AsCl3 + 6 Hg
- 2 As + 3 HgCl2 → 2 AsCl3 + 3 Hg
用途
[編輯]三硫化二砷可以用於製備砷單質[8]及三氧化二砷[9]、砷酸鹽[10]等其它砷化合物。
此外,三硫化二砷還能用作防腐劑,或在醫藥領域有所應用。[11]
安全
[編輯]As2S3不溶於水,因此毒性低。 老化的樣品中可能含有大量的砷氧化物,這些氧化物是可溶的,因此具有劇毒。
自然界的發生
[編輯]在火山環境中發現了雌黃,通常與其他硫化砷(主要是雄黃)一起被發現。 有時會在低溫熱液脈中發現它,以及一些其他硫化物和亞硫酸鹽礦物。
參考文獻
[編輯]- ^ 1.0 1.1 武漢大學 吉林大學等. 無機化學(第三版)下冊. 高等教育出版社, 2011. pp 704-706. ISBN 978-7-04-004880-3
- ^ Wells, A.F. (1984). Structural Inorganic Chemistry, Oxford: Clarendon Press. ISBN 0-19-855370-6.
- ^ 無機化學叢書. 第四卷 氮 磷 砷分族. 科學出版社. pp 408. 三硫化二砷
- ^ Arsenic sulfide (As2S3). [2020-06-11]. (原始內容存檔於2018-10-07).
- ^ Справочник химика. Редкол.: Никольский Б.П. и др.. (3-е изд.). испр. — Л.: Химия, 1971. Т. 2. pp 1168.
- ^ 鄭雅傑, 劉萬宇, 白猛. 採用硫化砷渣製備三氧化二砷工藝. 中南大學學報:自然科學版, 2008. 39(6): 1157-1163
- ^ 7.0 7.1 7.2 陳壽椿. 重要無機化學反應. 上海科學技術出版社, 1994
- ^ 侯漢娜, 陳甜甜. 硫化砷渣全濕法製備單質砷的研究. 環境保護科學, 2014(6):42-45
- ^ 孟文杰, 施孟華, 李倩 等. 硫化砷渣濕法製取三氧化二砷的處理技術現狀. 貴州化工, 2008, 33(5):26-28
- ^ 賴建林, 李勤. 用硫化砷渣製取砷酸銅. 有色金屬:冶煉部分, 2001, 1(2):42-44
- ^ 曹夢曄, 鞏江, 高昂 等. 雌黃藥學研究概況. 遼寧中醫藥大學學報, 2011(3):54-56

