乙酸鋇
| 乙酸鋇 | |
|---|---|
| |
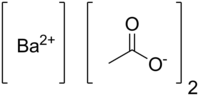
| IUPAC名 Barium acetate | |
| 英文名 | Barium acetate |
| 別名 | 醋酸鋇 |
| 識別 | |
| 縮寫 | Ba(OAc)2 |
| CAS號 | 543-80-6 |
| PubChem | 10980 |
| ChemSpider | 10515 |
| SMILES |
|
| InChI |
|
| InChIKey | ITHZDDVSAWDQPZ-NUQVWONBAA |
| EINECS | 208-849-0 |
| RTECS | AF4550000 |
| 性質 | |
| 化學式 | C4H6BaO4 |
| 摩爾質量 | 255.42 g·mol−1 |
| 外觀 | 白色固體 |
| 氣味 | 無味 |
| 密度 | 2.468 g/cm3(無水) 2.19 g/cm3(一水) |
| 熔點 | 450 °C(723 K) |
| 溶解性(水) | 55.8 g/100 mL (0 °C) 72 g/100mL (20 °C) |
| 溶解性 | 微溶於乙醇 |
| 磁化率 | -100.1·10−6 cm3/mol (2H2O) |
| 結構 | |
| 晶體結構 | tetragonal |
| 危險性 | |
GHS危險性符號
| |
| GHS提示詞 | 警告 |
| H-術語 | H302, H332[1] |
| P-術語 | P261, P264, P304+P340, P301+P312, P312, P501[1] |
| 致死量或濃度: | |
LD50(中位劑量)
|
921 mg/kg(大鼠,口) |
| 相關物質 | |
| 其他陰離子 | 甲酸鋇 硬脂酸鋇 |
| 其他陽離子 | 乙酸鈣 |
| 相關化學品 | 碳酸鋇 |
| 若非註明,所有數據均出自標準狀態(25 ℃,100 kPa)下。 | |
乙酸鋇是鋇的乙酸鹽,化學式為,有時寫作或。乙酸鋇存在無水物、一水合物和二水合物,也能形成酸式鹽。[2]
製備[編輯]
- Ba(OH)2 + 2 CH3COOH → Ba(CH3COO)2 + 2 H2O
- BaCO3 + 2 CH3COOH → Ba(CH3COO)2 + H2O + CO2↑
- BaS + 2 CH3COOH → Ba(CH3COO)2 + H2S
用途[編輯]
乙酸鋇可以作為原料,用於製備鈦酸鋇[4]、錫酸鋇[5]等鋇化合物。
管制信息[編輯]
乙酸鋇在中國屬於「一般危險化學品」而受到管制;在日本有毒有害物質控制法和有毒有害物質條例中屬於「有害物質」而受到管制。
參考文獻[編輯]
- ^ 1.0 1.1 醋酸鋇 化學品安全技術說明書. ThermoFisher Scientific. [2017-08-20]
- ^ 顧學民 等. 無機化學叢書 第二卷 鈹 鹼土金屬 硼 鋁 鎵分族. 科學出版社, 2011. pp 147. 4.9.2 有機酸鹽. ISBN 978-7-030550-3
- ^ Barium acetate (頁面存檔備份,存於互聯網檔案館), hillakomem.com, retrieved 30 June 2009
- ^ 王長文, 沈君權, 膝元成. 正丁醇鈦—乙酸鋇水解法合成BaTiO3粉體的工藝研究 (頁面存檔備份,存於互聯網檔案館)[J]. 武漢理工大學學報, 1994(1):7-12.
- ^ 王紅軍, 朱光輝, 郭書培,等. BaSnO3納米粒子的合成、表徵及其對甲基橙的光催化降解性能[J]. 信陽師範學院學報:自然科學版, 2013, 26(1):113-116.
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||




