醚


乙醚是一種常見的醚类,它常用于有机溶剂与医用麻醉剂。由于其在化学中的常用性(乙醚是最常用的醚类溶剂),我们还有时将乙醚直接简称为“醚”。結構最簡單的醚类是二甲醚 。醚类化合物的应用常见于有机化学和生物化学,它们还可作为糖类和木质素的连接片段。
结构和化学键
[编辑]醚的结构通式为:R-O-R(R')、Ar-O-R或Ar-O-Ar(Ar')(R=烃基,Ar=芳烃基)。醚的键角约为110°,C-O键长为140pm,C-O键的旋转能垒的能量很小,而水、醇与醚分子中氧的键合能力也与此相似。根据价键理论,氧原子的杂化状态是sp3。
氧原子的电负度比碳更强,因此与氧连接的α氢原子酸性强于碳连接的α氢原子,然而其酸性比不上羰基α氢原子。
分类
[编辑]醚可以根据醚键是否成环分为直链醚和环醚两大类。
分子中含有多个乙烯氧基(-CH2CH2O-)结构单元的大环醚称为冠醚。冠醚是一种大环多醚,因分子形状类似王冠而得名。
在直链醚中,氧原子所連結的兩個烴基相同者被稱為单醚,不同者被稱為混醚,若含芳基者則被稱為芳香醚。
命名
[编辑]| 外部圖片链接 | |
|---|---|
醚的普通命名法是于烃基后加上“醚”字,习惯上对称醚的“二”字可省略。醚的两个不同基团排列顺序通常是:先小基团后大则为:苯基或芳烃基在前。英文命名则按字母顺序。
遇到复杂的直链氧时,使用烃氧基(如烷氧基、烯氧基、苯氧基等)官能团命名。例如,“1,2-二(1-丙烯氧基)乙烷”(1,2-di(1-propenoxy)ethane)、“1,2-双(烯丙氧基)乙烷”(1,2-Bis(allyloxy)ethane)等等。
环醚则使用氧杂环命名法命名,但氧杂环丙烷通常用环氧基作用到烷烃的方式命名。遇到对称的冠醚时,还可命名为 x-冠-y,x代表环总原子数,y代表环中氧原子数。
物理性质
[编辑]醚分子不能互相形成氢键,因此它们具有和醇类相比较低的沸点。醚具有微弱的极性,这是由于醚官能团中碳氧碳的键角约110度,而碳氧之间的极性差异没有抵消(不同于二硫化碳之类的线型分子)。醚类极性不如醇、酯与酰胺类化合物,但是强于烯烃的极性。醚氧原子的孤电子对使它有可能与水分子形成氢键。
环状醚类比如四氢呋喃和1,4-二噁烷能与水混溶,这是因为这类醚分子的氧原子比起烷基醚(链状醚)来说更暴露于分子之外,所以极性比起后者更大。
| 常見烷基醚的理化数据 | |||||
|---|---|---|---|---|---|
| 醚 | 结构 | 熔点(°C) | 沸点 (°C) | 一升水当中的溶解度 H2O | 偶极矩 (D) |
| 甲醚 | CH3-O-CH3 | -138.5 | -23.0 | 70 g | 1,30 |
| 甲乙醚 | CH3-O-CH2CH3 | -113 | 7.4 | ||
| 乙醚 | CH3CH2-O-CH2CH3 | -116.3 | 34.4 | 6.9 g | 1.14 |
| 正丁醚 | C8H18O | −95 | 141 | 0.3 | |
| 叔丁醚 | C8H18O | −61 | 107.2 | ||
| 甲基叔丁基醚 | C5H12O | −109 | 55.2 | 42 | |
| 四氢呋喃 | O(CH2)4 | -108.4 | 66.0 | 互溶 | 1.74 |
| 二氧六环 | O(C2H4)2O | 11.8 | 101.3 | 互溶 | 0.45 |
反应
[编辑]
醚类总体来说化学活性都较低,但强于烷烃(环氧化物、酮、缩醛参见各自条目)。
与醚相关的重要反应讲解如下:[3]
醚的裂解
[编辑]虽然醚不能轻易的发生水解反应,但于酸性条件下(如:氢溴酸或氢碘酸),可断裂为醇。盐酸条件下,断裂醚的速度非常慢。如:甲醚制备溴化甲烷:
- ROCH3 + HBr → CH3Br + ROH
该类反应都是通过鎓中间体进行,如:[RO(H)CH3]+Br-.
有些醚类能于三溴化硼条件中迅速分解,有时还可用更强的路易斯酸如:三氯化铝反应,制备溴代烷烃。[4]这些都取决于取代基的不同,还有些醚类可在特定的试剂中发生裂解,如非常强的碱。
过氧化物
[编辑]临近氧原子,含有CH基团的一级醚或二级醚易形成有机过氧化物,如:乙醚过氧化物。该反应需要氧气(或者空气)参与,且在光、金属和醛的催化下加速反应。得到的过氧化物在高温或高浓度下具爆炸性,因此操作二异丙基醚、四氢呋喃等醚类溶剂大多都不可蒸干,而厂商在分装醚类试剂也会放入一些稳定剂,防止大量产生过氧化物。
作为路易斯碱
[编辑]醚类可作为路易斯碱及布仑斯惕碱。强酸与醚发生反应,可提供给醚氧原子一个质子,从而形成:“鎓离子”,如:乙醚可以与三氟化硼形成络合物(BF3.OEt2) 。醚还可与二价镁络合成格氏试剂。多聚醚都可与碱金属离子牢固的结合。
α-卤化反应
[编辑]该反应类似于醚的α氢原子发生过氧化的反应,如:单质氯制备α-氯化醚的反应。
合成
[编辑]醚在实验室条件下可通过许多方法合成,以下枚舉數種。
醇的脱水
[编辑]- 2 R-OH → R-O-R +H2O(高温下)
该反应过程需要高温(通常在125°C)。该反应还需要酸的催化(通常为硫酸)。上述方法对于制备对称醚来说有效,但对于不对称醚却无能为力,如:乙醚易于通过此法制备,环醚也同样可用此方法制备(分子内脱水)。另外此方法还会引入一定的副产物,如分子内脱水产物:
- R-CH2-CH2(OH) → R-CH=CH2 + H2O
另外此法只能合成一些简单的醚,对于复杂的分子醚类分子不太试用。对于复杂分子则需要更温和的条件来合成。
威廉森醚合成
[编辑]- R-ONa + R'-X → R-O-R' + NaX
该反应称作:威廉姆逊合成。该反应通过用强碱处理醇,形成醇盐,而后与带有合适离去基团的烃类分子反应。这里的离去基团包括:碘、溴等卤素,或磺酸酯。该方法对于芳香卤代烃一般不适用(如:溴苯,参见Ullmann缩合)。该方法还只局限于一级卤代烃才可得到较好的收率,对于二级卤代烃与三级卤代烃则由于太易生成E2消除产物而不适用。
在相似的反应中,烷基卤代烃还可与酚负离子发生亲核取代反应。R-X虽不能与醇反应,但酚却能够进行该反应(酚酸性远高于醇),它可通过一个强碱,如:氢化钠先形成酚负离子再进行反应。酚可取代卤代烃中的X离去基团,形成酚醚的结构,该过程为SN2机理。
- C6H5OH + OH- → C6H5-O- + H2O
- C6H5-O- + R-X → C6H5OR
Ullmann二芳醚合成
[编辑]Ullmann二芳醚合成的反应很类似于威廉姆逊反应,不同之处在于底物是芳香卤代烃。该反应需要催化剂才能进行,如:铜。
醇对于烯烃的亲电加成反应
[编辑]醇可与活化后的烯烃进行亲电加成:
- R2C=CR2+ R-OH → R2CH-C(-O-R)-R2
该反应需要酸催化,三氟醋酸汞(Hg(OCOCF3)2)常可作为这种反应的催化剂,反应生成具有弗拉基米尔·瓦西里耶维奇·马尔科夫尼科夫(Markovnikov)立体化学的醚类。使用相似的反应条件,四氢吡喃醚(THP)可作为一种醇的保护基。
制备环氧化合物
[编辑]环氧化合物通常由烯烃氧化制备。在工业生产中,最重要的环氧化合物是:环氧乙烷,它通过乙烯和氧气制备。其他的过氧化合物还可通过以下方法制备:
重要的醚
[编辑]
|
环氧乙烷 | 最小的环状醚。 |
| 甲醚 | 一种新型的可再生替代燃料,可以和十六烷以一定的比例混合作为柴油内燃机的燃料。 | |
| 乙醚 | 一种常用的低沸点溶剂 (沸点:34.6°C),早期用作麻醉剂。可以用作启动柴油发动机的燃料。 | |

|
二甲氧基乙烷(DME) | 一种高沸点溶剂 (沸点为 85°C)。 |

|
二氧六环 | 一种高沸点的环状的醚 (沸点为101.1°C)。 |

|
四氢呋喃(THF) | 一种环状醚类,是有机合成当中极性最大醚类溶剂之一。 |

|
茴香醚(苯甲醚) | 一种“芳香醚”,是大茴香种子精油的主要组分。 |
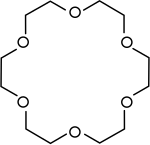
|
冠醚 | 环状多聚醚用来做相转移催化剂。 |

|
聚乙二醇(PEG) | 一种线形的多聚醚,可以用作化妆品添加剂或者药物材料(其具有高水溶性,可以让一些非水溶性分子大大增加水溶性)。 |
参考文献
[编辑]- ^ 國際純化學和應用化學聯合會,化學術語概略,第二版。(金皮書)(1997)。在線校正版: (2006–) "ethers"。doi:10.1351/goldbook.E02221
- ^ ([//web.archive.org/web/20230311001802/https://pubchem.ncbi.nlm.nih.gov/compound/2-_Phenoxy_prop-2-enoxy_methyl_oxirane 页面存档备份,存于互联网档案馆) 2-[苯氧基(丙-2-烯氧基)甲基]氧杂环丙烷 - PubChem]
- ^ Heitmann, Wilhelm; Strehlke, Günther; Mayer, Dieter. Ethers, Aliphatic. Wiley-VCH Verlag GmbH & Co. KGaA (编). Ullmann's Encyclopedia of Industrial Chemistry. Weinheim, Germany: Wiley-VCH Verlag GmbH & Co. KGaA. 2000-06-15: a10_023. ISBN 978-3-527-30673-2. doi:10.1002/14356007.a10_023 (英语).
- ^ J. F. W. McOmie and D. E. West (1973). "3,3'-Dihydroxylbiphenyl". Org. Synth.; Coll. Vol. 5: 412.
外部連結
[编辑]- ILPI page about ethers.
- An Account of the Extraordinary Medicinal Fluid, called Aether (页面存档备份,存于互联网档案馆), by M. Turner, circa 1788, from Project Gutenberg

